Pregabalin
Il Pregabalin è un antiepilettico-anticonvulsivante che trova indicazione specifica nel trattamento del dolore neuropatico centrale e periferico.
| Pregabalin | |
|---|---|
 | |
 | |
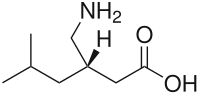
| Nome IUPAC | |
| acido (S)-3-(amminometil)-5-metilesanoico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C8H17NO2 |
| Massa molecolare (u) | 159,23 g/mol |
| Numero CAS | |
| Numero EINECS | 604-639-1 |
| Codice ATC | N03 |
| PubChem | 5486971 |
| DrugBank | DBDB00230 |
| SMILES | CC(C)CC(CC(=O)O)CN |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | 1.13e+01 |
| Dati farmacologici | |
| Modalità di somministrazione | orale |
| Dati farmacocinetici | |
| Emivita | 5-6,5 ore |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 318 - 361 |
| Consigli P | 280 - 305+351+338 [1] |
È utilizzato anche contro il disturbo d'ansia generalizzato (GAD), e contro il dolore neuropatico periferico causato da complicanze dell'algodistrofia (o distrofia simpatica riflessa).
È commercializzato da Pfizer come nome commerciale di Lyrica in dosaggi che partono da 25 mg fino a un massimo di 300 mg.
Meccanismo d'azione
Il pregabalin si lega ai canali del calcio voltaggio-dipendenti diminuendo l'attività di numerosi neurotrasmettitori come glutammato, noradrenalina, sostanza P. Non è in grado di interferire positivamente con l'attività del GABA, a differenza di gabapentin e benzodiazepine.
Effetti collaterali attesi
- In seguito alla sospensione del trattamento con pregabalin può comparire sindrome da astinenza[2].
- Il trattamento con pregabalin è stato associato a cambiamenti dell'umore, a comparsa di depressione fino a ideazione e comportamenti suicidari. Da una revisione condotta sui farmaci antiepilettici dalla FDA è stato evidenziato un lieve rischio di ideazione e comportamento suicidario associato alla terapia antiepilettica. I farmaci oggetto dello studio sono stati: carbamazepina, felbamato, gabapentin, lamotrigina, levetiracetam, oxacarbazepina, pregabalin, tiagabina, topiramato, valproato, zonisamide. Sono stati valutati gli studi clinici verso placebo in cui i farmaci antiepilettici sono stati impiegati per il trattamento dell'epilessia e altre patologie, inclusi disturbi psichiatrici. Sulla base dei dati disponibili, l'uso di un farmaco antiepilettico aumenta il rischio di pensieri e comportamenti suicidari di circa 2 volte rispetto al placebo (0,43% vs 0,22%). Tale rischio può manifestarsi già dopo una settimana di terapia e si mantiene per 24 settimane[3].
- Durante la sorveglianza post-marketing il pregabalin è stato associato ad episodi di scompenso cardiaco in pazienti con malattia cardiovascolare, in trattamento con l'antiepilettico per il dolore neuropatico[4][5][6].
- Il pregabalin è classificato come un farmaco con un basso potenziale di abuso. Questo non esclude comunque che possa essere utilizzato come tale, soprattutto in pazienti con storia di abuso[7][8].
- Sono riportati in letteratura casi rari di encefalopatia dopo interruzione improvvisa del pregabalin anche in pazienti non epilettici. La possibilità che si sviluppi edema focale vasogenico in seguito ad interruzione repentina della terapia antiepilettica è un evento noto. Una condizione simile è stata riportata in un paziente non epilettico in terapia con pregabalin per il trattamento del dolore neuropatico conseguente a nevralgia posterpetica. L'interruzione improvvisa del pregabalin ha indotto la comparsa, 30 ore più tardi, di nausea, cefalea, atassia che sono progrediti fino a delirio 8 giorni dopo. La risonanza magnetica ha evidenziato la presenza di lesioni a livello dello splenio del corpo calloso simili a quelle riscontrate in caso di edema cerebrale da alta quota (High-Altitude Cerebral Edema)[9].
Controindicazioni
Controindicata in caso di allattamento
Dosaggi
- Dolore neuropatico, 150 mg diviso in due.
Effetti indesiderati
Fra gli effetti collaterali più frequenti si riscontrano edema, parestesie, vertigini, dispnea, tachicardia, diplopia, insonnia, vomito, secchezza delle fauci, disturbi della memoria
Note
- ^ Sigma Aldrich; rev. del 23.03.2013
- ^ Scheda Prodotto LYRICA, disponibile on line http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/000546/human_med_000894.jsp&murl=menus/medicines/medicines.jsp&mid=WC0b01ac058001d124
- ^ FDA, Postmarket Drug Safety Information for Patients and Providers, 2008, 31 gennaio
- ^ Page R.L. et al., J. Cardiovasc. Med. (Hagerstown), 2008, 9 (9), 922
- ^ De Smedt R.H. et al., Br. J. Clin. Pharmacol., 2008, 66 (2), 327
- ^ Laville M.A. et al., Rev. Med. Interne, 2008, 29 (2), 152
- ^ Filipetto F.A. et al., J. Am. Osteopath. Assoc., 2010, 110 (10), 605
- ^ Schwan S. et al., Eur. J. Clin. Pharmacol., 2010, 66 (9), 947
- ^ Oaklander A.L., Buchbinder B.R., Ann. Neurol., 2005, 58 (2), 309
Bibliografia
- British national formulary, Guida all’uso dei farmaci 4 edizione, Lavis, agenzia italiana del farmaco, 2007.